勉強時間 昨日11.5H 今日13H
今月はお誕生日月と言うこともあり、買っちゃいました。
バーローは上下巻で購入。アトキンスも個人的には良いなと思ったのですが、レビューを見ると誤訳が多いとのことだったので、より評判の良かった方にしました。
無機化学は、そもそもまだ岡野シリーズが無機化学に入っていないので、無機化学の勉強を本格的にスタートする前、4月1週目までには購入します!
<勉強内訳>
・トライアルシリーズ見直し+C視聴完 7H
・化学 4H
・物理 1.5H
・ガスクロ 情報収集 0.5H
●トライアルレビューシリーズ
Cシリーズ視聴。差を見る。
反応が追っかけられていない、化合物の掛かりが間違っている、と言うところは無さそうでした。ただ専門用語の訳し方に難あり。
日本語ではあまりこう言わないけど英文側がこうだから則して訳すか、と判断したところが微妙な訳になっている感じでした。とりあえず某翻訳会社さんのブログを元に勉強していきながら、化学の勉強時にも英文の使い方を確認することを心掛けていこうと思います。後は日本語インプット。
●化学
TC0132_岡野の化学(132)中和滴定 途中から
TC0133_岡野の化学(133)演習問題
TC0134_岡野の化学(134)酸化還元 途中まで
中和滴定とは
濃度が分からない酸性(塩基性)の溶液に濃度の分かっている塩基性(酸性)の溶液を少量ずつ加えて中和点を確認し、酸性の溶液の濃度を決める操作。
水のイオン積は以下のように求められることから、
HとOHの積は、常に10の-14乗になるので、片方が決まれば必然的に片方も決まる。
水のイオン積Kw=[H+]×[OH-]= 1.0×10-14(mol/L)2
よって、試料中の成分量を決定する定量分析に使うことができる。
その他メモ
※酸性溶液と塩基性溶液の強弱によっては中和する当量点が中性とは限らない。
→・強酸と強塩基→作られた塩:中性。よって液も中性(pH=7)
・強酸と弱塩基→作られた塩:酸性。よって液も酸性(pH<7)
・弱酸と強塩基→作られた塩:塩基性。よって液も塩基性(pH>7)
※中和点と溶液の濃度は関係するのか?
→滴下する溶液の濃度が変わってしまうと、算出する被測定溶液の値を正確に計算できなくなる。
だから実験前にはビュレットなどを共洗いする必要がある
※酢酸とNAOHの中和滴定を行った場合に中和を過ぎて少し色が変わった溶液をそのまま放置しておくと、色が消えるのはなぜか?(知恵袋にあった質問)
*状況分析*
中和点を過ぎて少し色が変わっている状態の溶液は、今回弱酸と強塩基の反応であるため、少し塩基性寄りになっていると考えられる。それが酸性に戻るのはなぜか?と言うのが質問者の状況。
→知恵袋の解答① 「時間が経つと拡散するから」
拡散は蒸発の意味で使っているのかな?と想定。
蒸発して酸化が進む場合、蒸発するのは塩基性の水酸化ナトリウム水溶液になる。
水酸化ナトリウムは揮発性ではなく、空気中に存在しにくい物質、と言われている。
よって、これはあまり考えにくい気が個人的にはする…
→知恵袋の解答② 「空気中の二酸化炭素が溶けるから」
二酸化炭素は空気より重いので可能性としてはあり?
Chemstation曰く、二酸化炭素はアルカリ水溶液に吸収されやすい、とのこと。
個人的にはこれが有力と考えた。
●物理
TP0069_橋元・物理基礎(69)~振動の正体
音は空気の振動によって伝わる→音源から音が出ると、その周辺の空気が圧縮して密になる。
密になった空気はさらに隣の空気を押す(圧縮した空気が戻ろうとするために隣の空気を押すのかなと思う)
この空気の疎密波が、空気中に拡がって誰かの耳へと届くと音が聞こえる。
ちなみに、
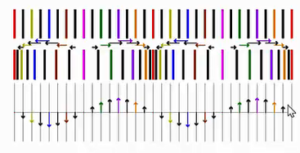
http://wakariyasui.sakura.ne.jp/p/wave/hadou/yokotate.html
こちらの縦波と横波の図では、一番密の部分に波の腹が来ていませんね…。
やっぱり誤りですよね。
正しくは、↓こんな感じの波になるはず。
<3/9追記>
上の図は、疎密波を表しているのではなく変位量を波形にした図なんですね。
上の図では疎の部分の矢印が長くなるので、その部分の波の腹が高くなっています。
で、こちらの下の図が疎密波を表した図です。なので音が一番大きくなる密の部分の波の腹が盛り上がっています。
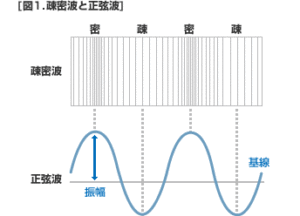
参照:https://www.widexjp.co.jp/hearing/various_sounds/
上の図と下の図は別のものをグラフ化しているわけですから同じでなくて当然ですね。
———————————————————-
<明日やること>
・化学
・物理
・トライアルシリーズ
・分析装置の情報収集


コメントを残す